A tudásvágy sikert hoz: Alessandro Volta
2010/12. lapszám | Chiovini György | 14 998 |
Figylem! Ez a cikk 16 éve frissült utoljára. A benne szereplő információk mára aktualitásukat veszíthették, valamint a tartalom helyenként hiányos lehet (képek, táblázatok stb.).
A ma használatos mértékegységeket híres személyekről nevezték el. A feszültség mértékegysége a volt, névadója Alessandro Volta, olasz fizikus. Valóban meghatározó szerepe volt az elektrotechnika fejlődésében, mert ő készített először egy gyakorlati alkalmazásra is jól megfelelő áramforrást. Ez azért történhetett így, mert Volta mindenáron tisztázni akart egy különös jelenséget. Hosszú éveket töltött kísérletekkel, vitatkozott az észlelt jelenségek magyarázatáról. Végül jött a döntő gondolat, azután a siker, az elismerés.
 |
Mi történik a békával?
A villamos energiával működő eszközeinket feloszthatjuk hálózatról tápláltakra és hálózattól függetlenekre. Ez utóbbiakhoz nincs szükség egy közelben lévő dugaszolóaljzatra és csatlakozó vezetékre. A használati idő azonban véges, az eszközben lévő áramforrástól függ. Tudjuk, hogy a fejlesztők óriási erőfeszítéseket tesznek, hogy minél jobb tulajdonságú, minél nagyobb energiatároló képességű áramforrásokat hozzanak létre.
Eközben nem is nagyon gondolunk arra, hogy az elektromosság gyakorlati alkalmazása is „hordozható” áramforrásokkal kezdődött. A tudósok már régen foglalkoztak a természetben fellépő óriási energiájú villamos áramokkal, a villámokkal. Az amerikai Benjamin Franklin 1752-ben mutatta be találmányát, a villámhárítót. Létrehozni ebben a történeti időszakban azonban – mai szemmel nézve – csak nagyon kis áramokat tudtak. Dörzsöléssel vil- lamos töltéseket halmoztak fel, és a töltés-kiegyenlítődés során rövid ideig nagyon kis erősségű áram folyhatott. Ez látványos kísérletekre jó, hasznos alkalmazásra nem megfelelő volt. Nem is nagyon gondolt senki arra, hogy a villamosság egyszer milyen kulcsszerepet játszik majd a mindennapi életben. Ehhez a jelenségek okát kutató emberi természetre, az észlelt jelenségekre magyarázatot kereső természettudósokra volt szükség. Ilyen volt az olasz Alessandro Volta. Volta figyelmét felkeltette orvos honfitársa, Luigi Galvani beszámolója egy általa észlelt különös jelenségről.
Ezt a nevezetes békacombos esetet gyakran idézik a technikatörténetben. Galvani egy véletlen folytán azt vette észre, hogy a laboratóriumban lévő békacomb – mintha áramütés érte volna – megrázkódott. Ez felkeltette kíváncsiságát, és alaposabban meg kívánta vizsgálni a jelenséget. Abban az időben a kísérletekhez jól jött az „égi segítség” is, Galvani békacombokat akasztott az ablak vasrácsára. Kíváncsi volt, villámlás esetén is észlehető-e a békacomb rázkódása. Anélkül, hogy villámlott volna, a békacombok megrázkódtak, amikor a szél a rézkampón függő testrészt a vasrácshoz lendítette. Galvani úgy vélte, hogy az „áramforrás” a béka szervezetében van, csak az áramkör záródásához kellett a vasrácshoz érnie. Abban az időben már ismerték és tanulmányozták a villamos képességekkel rendelkező állatokat, például a rájákat. Galvani elgondolása tehát elfogadhatónak tűnt. Volta viszont kételkedett abban, hogy a jelenség oka az „állati elektromosság”. Feltételezte, hogy nagyobb jelentőségű a két különböző fém jelenléte. Sok kísérletet végzett különböző fémekkel. Így jutott el ahhoz az alapvető megállapításhoz, hogy a békacombok – mai szakkifejezéssel – sós elektrolitokat jelentettek a fémek számára. A rézből, vasból és békából összeállított „bio-áramforrás” lépett működésbe, amikor az áramkör a szél hatására záródott. A béka teste a külső eredetű áram élettani hatására rándult meg.
Volta korszakalkotó felismerése az volt, hogy a békacomb helyett alkalmas elektrolitot kell keresni, és akkor egy addig nem létező, nagyszerű áramforráshoz lehet jutni. El is készítette ezt az áramforrást, a róla elnevezett Volta-elemet, majd a Volta-oszlopot. A Volta-elem alkotórészei: üvegedényben kénsav, ebbe merülő réz, illetve cink elektróda. A Volta-elem névleges feszültsége 1,1 volt volt, de az elemeket sorba kötve a feszültségek összegződnek. Volta kezdetben egyszerűen a kis kénsavas edénykéket kapcsolta össze. További nagyszerű gondolata az volt, hogy a folyadék használatát is kiküszöbölte. Cink és réz anyagú tárcsák közé elektrolittal átitatott papír- vagy szövetdarabokat helyezett. Ezekből az egységekből oszlopot állított össze (4. ábra). A tárcsák számával arányosan egyre nagyobb feszültségű áramforrás készíthető. Abban az időben egy áramforrást persze nem digitális multiméterrel teszteltek. Figyelemre méltó egy akkori leírás a Volta-oszlop érzékszervi úton történő tanulmányozásáról: „Ha pl. a positiv sarkot az egyik kézzel, a negativ sarkot pedig a másikkal érintjük, rázkodást érzünk, mely a leydeni palaczktól okozotthoz hasonló; ezt követőleg, ha az érintkezés még tovább tart, kezeinkben különös melegítő hatást és berzengést érzünk. Ha az oszloppal érintkező végtagokon a legcsekélyebb metszés vagy karczolás van, a sérült helyen oly fájdalmas érzés tapasztalható, melyet alig lehet elviselni.”
 |
Az elem, mint energiaátalakító
Ismerjük az energia-megmaradás törvényét. Ha a Volta-elem áramot szolgáltat, honnan származik ez az energia? Az a válasz, miszerint kémiai energia alakul át villamos energiává, igaz, de kissé semmitmondó. A felelethez célszerű megismerni a Volta-elem működését. Logikus az, hogy a külső áramkörben mozgó töltéshordozók, az elektronok az egyik elektródából kell, hogy származzanak, és a másik elektróda nyeli el őket. A Volta-elemnél az elektronforrás a cink elektród, az elektronnyelő a réz elektród (3. ábra). A cink ugyanis jól oldódik a kénsavban.
Az elektródból a cink pozitív töltésű ion formában válik ki, negatív töltésű elektronokat hagyva hátra. A kénsav hidrogén- és szulfátionok formájában van jelen. A hidrogénionok a rézelektródon elektronokat vesznek fel, és hidrogénmolekulákká állnak össze. Tehát a két elektród és a kénsav közötti kémiai folyamatok az egyik helyen elektron- többletet hoznak létre, a másik helyen elektron- felvétel megy végbe. Még egy kiegészítés: a cink inkább oldódik, mint a réz, ezért a cink válik elektrontermelővé, nem a réz. Ennek az elvnek az alapján akár a konyhaasztalon is készíthetünk egy elektrokémiai áramforrást, például citromból. Kell hozzá két különböző fém, választhatunk alumíniumot, rezet, vasat, és természetesen egy citrom.
Ha a két fémet úgy szúrjuk bele a citromba, hogy egymással nem érintkeznek, már mérhetjük is az SK-elem feszültségét. Egy hasonló tanulságos kis barkácsoláshoz alufólia és egy rézérme (rézlemez) szükséges. Az alufóliát az egyik, a rezet a másik kezünkbe fogjuk. A bőrünk mindig egy kissé nedves, ezáltal mi leszünk a „belső áramkör”, akár Galvani professzor békája. Ha éppen megizzadtunk, és sós a bőrünk, az „elem” nagyobb feszültséget ad le.
Megszületik a tartós elem
Ma természetes, hogy gyakorlatilag bárhol használhatjuk a villamos energiát igénylő eszközeinket. Az áramszünet ijesztő lehetőség. Micsoda szenzáció lehetett annak idején, hogy Volta találmányával már különösebb előkészület nélkül rendelkezésre állt a villamos energia. Ezt emelte ki Volta is, amikor bemutatta a Volta-oszlopot: „Amiben azonban mindenekelőtt végtelenül felülmúlja ezeknek a battériáknak jelességét és erejét, az az, hogy szemben amazokkal, nincs szükség előzetes feltöltésre külső elektromosságból, továbbá az, hogy bármikor, bármely gyakran bekapcsolva kifejtheti hatását.” Az Alessandro Volta által létre hozott áramforrások óriási lökést adtak az elektrotechnika, elsősorban az elektrokémia fejlődésének. Nem csak jól hangzik, de igaz is, hogy a Volta-oszlop nagyszerűségét egyszerűsége adta. Egyszerűen összeállítható volt, akár réz és ezüst pénzérmékből is. Azonnal alkalmazni kezdték, és igen eredményesen. Orvosok alkalmazták a gyógyászatban.
Természettudósok előállítottak vele egy sor olyan elemet, mint kalcium, kálium, nátrium. Használták elektrolizálásra, nemesfém bevonatok készítésére. Hatalmas, több négyzetméter felületű Volta-oszlopokat is készítettek. Ezek olyan áramerősség leadására voltak képesek, hogy a két kivezetésük közé iktatott fémrúd izzásig hevült. A Volta-oszlop lényeges fogyatékossága azonban az, hogy viszonylag gyorsan kimerül, az áramerősség folyamatosan csökken. Ennek oka lényegében az, hogy az elektródokon káros folyamatok mennek végbe. Az elektrolitból kiváló hidrogén a cink felületén gyűlik össze. Az oldatba kerülő cinkionok a réz elektródon kiválnak. A megoldás az, hogy az elektródáktól tartsuk távol ezeket a reakciótermékeket. A francia fizikus, Antoine-César Becquerel, különben a Nobel-díjas Henri Becquerel nagyapja, 1829-ben azt javasolta, hogy az elektródokat fizikailag különítsék el, de az ionvándorlást közöttük tegyék lehetővé.
 |
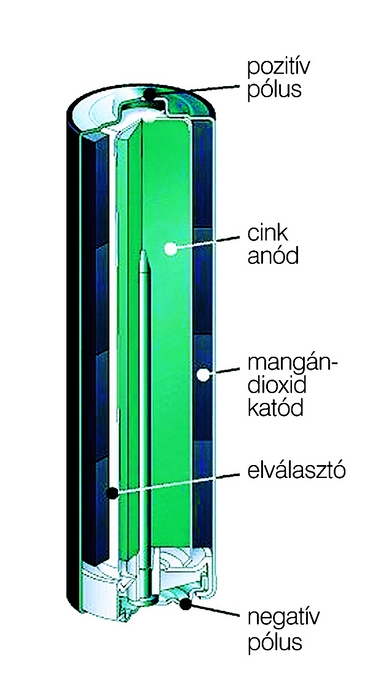
Ennek megoldása lehet olyan elválasztó réteg, mely bizonyos ionokat átenged, másokat visszatart. 1866-ban szabadalmaztatta a francia Georges Leclanché a cink-szén, pontosabban cink-mangán galvánelemet. Az elv annyira időtálló, hogy az eredetihez közeli változatát ma is használjuk, és tovább- fejlesztett változata – az alkáli elem – megfelel a mai elvárásoknak is. A német Carl Gassner 1886-ban kapott szabadalmat egy tökéletesített cink-szén elemre. Mint a lakáscsengők áramforrása, Németországban oly mértékű volt a kereslet, hogy külön gyárat építettek az előállítására. Egy további fontos szempont volt a fejlesztésnél, hogy a folyékony elektrolitot kiküszöböljék. Így jött létre a szárazelem, melynek elektrolitja pép vagy kocsonyás alakban, illetve valamilyen nedvszívó anyag által megkötött állapotban van, és így az elemből nem folyik ki. A „klasszikus” cink-szén (cink-mangán) elemben az anód a cink, a katód szénporral kevert mangán-dioxid (barnakő) egy kivezetésül is szolgáló szénrúddal egyesítve (1. ábra). A cink anód egyben az elem háza is.
A házat az elektrolit, kocsonyásított ammónium-klorid oldat tölti ki. Ezt aszfaltréteg zárja le, mely villamosan szigetel a ház és a szénrúd között. A cink az elektronkibocsátó, a mangán-dioxid az elektron felvevő. A kisütés közben a cink, a mangán-dioxid és az elektrolit elhasználódik. A cink-szén elemek azért kedveltek, mert olcsók. Viszont előfordul, hogy a töltet kiszivárog, tönkretéve elsősorban a csatlakozó érintkezőket, súlyosabb esetben azt az eszközt is, amiben az elemet használtuk. Ma a cink-szén elem legjobb változata az alkáli elem. Szokásos kereskedelmi megnevezése még: tartós elem. Arra utal ez, hogy az egyszerű cink-szén elemekhez képest „tartósabb”: hosszabb ideig számottevő önkisülés nélkül tárolható, illetve nagyobb a mAh-ban kifejezett kapacitása is. A fejlesztők számos szerkezeti módosítással érték el ezt. Az alkáli elem háza nem cinkből, hanem acélból van. A cink elektród, illetve a mangán-oxid elektród por alakú, ezáltal nagyobb felületű. Az elektrolit kálium-hidroxid, ebből ered az alkáli megnevezés, mert a kálium alkálifém (2. ábra). Az ilyen elektrolitnak jobb a vezetőképessége, ezáltal kisebb az elem belső ellenállása. A belső ellenállás fontos jellemző, mert minél kisebb a kisütő áramból és a belső ellenállásból számított feszültség, annál nagyobb a kapcsokon mérhető feszültség. Az elektródokat ionszelektív felület választja el egymástól. A cink-szén (cink-mangán) elem névleges feszültsége 1,5 volt. A gyakorlatban nagyon elterjedtek a három elemből összeállított 4,5 voltos telepek, illetve a hat elemből álló 9 voltos telepek.
 |
Fény és árnyék
Az elektrokémiai áramforrások, azok közül is a galvánelemek, valóban megkönnyítik életünket. Eredményes és hatékony használatukhoz érdemes néhány dologgal tisztában lenni. Nagy piacról van szó, a gyártók mindent elkövetnek, hogy termékeik vásárlására ösztönözzék a vevőket. Ezt inkább ügyes reklámfogásokkal, mint részletes tájékoztatással igyekeznek elérni. Az elemek legfontosabb műszaki jellemzői: névleges feszültség, legnagyobb megengedett áram, alkalmazási hőmérséklet, kapacitás, önkisülés. A kapacitás függ a kisütéstől, a kisütő áramerősségtől. Ha nagyobb árammal történik, a kivehető energia kisebb.
Két elem kapacitását csak úgy lehet összehasonlítani, ha azonos módon történik a kisütésük. Egy olcsó micro méretű (O10,3x45 mm) cink-szén elem kapacitása néhány száz mAh, egy nagy teljesítményű alkáli mono (O35x62 mm) elem kapacitása hozzávetőlegesen húszezer mAh. Szoros összefüggés van az önkisülés és a használat előtti tárolhatóság között. A legjobb tartós elemekre a gyártó hét év tárolhatóságot ad meg. Az elemeknél két jelölési rendszer létezik egymás mellett.
A szokásos kereskedelmi megnevezés mellett az ANSI, azt követően az IEC rendszer jelölése található (az „L” betű a tartós elemre utal, az „R” betű cink-szén elemet jelöl): micro/LR3,R3/AAA – mignon/ LR6, R6/AA – baby/LR14,R14/C – mono/ LR20,R20/D. Egy használt elem még létező kapacitását műszerrel vizsgálhatjuk. A feszültségmérő műszer nagy ellenállású, az elemet nem terheli, a mérőáram elhanyagolható. Ilyenkor az elektrokémiai működési elvből származó potenciálkülönbség jelenik meg az elem kivezetésein.
Ez állandó, nem jellemzi az elem kisütöttségét; természetesen a teljesen kisütött elemnél nem mérhető feszültség. Érdemi információhoz úgy jutunk, ha a mérést terhelés közben végezzük. Hozzávetőleges megállapításhoz még jobb módszer az, ha egy izzólámpát érintünk az elemhez. Ennek fényereje elég jól jellemzi, mennyire lett már kisütve az adott elem. Vannak olyan készülékek, melyek csak nagy áram leadására képes elemmel működnek. Ilyenek többek között a fényforrások (pl. zseblámpa, vaku) és a villamos motort tartalmazó készülékek (pl. fényképezőgép, ventilátor). Az ilyen célra már nem megfelelő elem más készülékben, ahol kisebb az igénybevétel, rendszerint még tovább használható (pl. hőmérő, számológép).
Előbb vagy utóbb minden elem kimerül, az elektrokémiai folyamatban résztvevő anyagok elfogynak. Az elemekben felhasznált anyagok egy része a környezetre és az emberi egészségre ártalmas. Ilyenek a toxikus nehézfémek és vegyületeik, többek között a cink.
Erre való tekintettel tilos a használt elemeket a lakossági hulladékba keverni, tehát a háztartási szemétgyűjtőbe (kukába) dobni. Az elemet a kereskedők visszafogadják, ez a visszafogadás ingyenes, és a kereskedő nem kötheti a visszavételt új termék vásárlásához. A begyűjtést követően az elemekből értékes nyersanyagokat lehet kinyerni. Kétszáz éve elkezdődött valami. Ma már nem gond, hogy a legkényesebb igénynek is megfelelő, hálózattól független elektrokémiai áramforráshoz jussunk.
Ellenkezőleg, gondot inkább az jelent, hogy miután az elem élettartama végére ért, ne a környezet szennyezője legyen, hanem új elemek gyártásához lehessen újrahasznosított anyagait felhasználni. Nagyon hosszú időn keresztül az elemek útja a szeméttelepekre vezetett, és maradványaik nehezen felbecsülhető kárt okoztak, okoznak az élővilágnak. Alessandro Voltához nem volt hálátlan az utókor. Szülővárosában, Comóban róla nevezték el a főteret. Paviában, ahol az egyetemen tanított, szobrot állítottak neki. Nevét őrzi a villamos feszültség egysége.
